Un revolucionario tratamiento contra el VIH ha sido elegido como el avance científico del año por la prestigiosa revista ‘Science’. Bautizado con el nombre de lenacapavir, este medicamento no solo ha demostrado una gran capacidad para combatir el sida, sino que tiene una impresionante capacidad para prevenir el contagio, total en el caso de las mujeres y de un 99,9% en hombres cisgénero, mujeres y hombres transgénero y personas de género no binario.
«Hace las funciones de una vacuna a corto plazo», enfatiza Luis Menéndez Arias, especialista del Centro de Biología Molecular Severo Ochoa. Según los expertos, estos resultados «abren un camino hacia la esperanza» para combatir un virus que fue identificado en 1983 tras detectarse los primeros casos en 1981 en California y Nueva York -en España fue en ese mismo año en Barcelona- y que afecta a 39 millones de personas en todo el mundo. Estas son las claves.
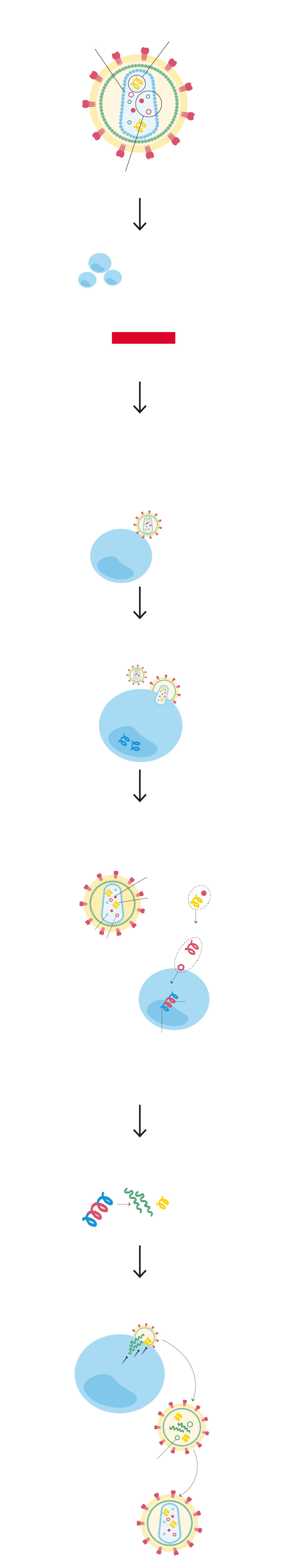
Cómo se reproduce el virus

(virus de la inmunodeficiencia humana)
ARN del virus
Enzimas necesarias para replicarse
– Transcriptasa inversa
– Integrasa
– Proteasa
INFECTA….
Células CD4
Tipo de linfocitos que activan el sistema inmunitario en caso necesario ante la presencia de infecciones u otras enfermedades.
INACTIVADORES (I)
Hay varias clases de medicamentos que inactivan el virus en diferente etapas de su ciclo de vida
Enlace.
El VIH se fija a los receptores en la superficie del CD4.
(I) Antagonistas de CCR5 (bloquean para que no entre el VIH)
(I) Inhibidores posfijación
Célula CD4
Fusión.
Permitiendo que el VIH entre en la célula.
(I) Inhibidores de la fusión
Transcripción inversa.
Esta enzima convierte el ARN del VIH en ADN, para así poder entrar en el núcleo del linfocito CD4.
(I) Inhibidores de la transcriptasa
ARN del virus
Transcriptasa inversa
ADN del VIH
ADN del VIH
ADN de la CD4
Integración en el genoma del huésped (CD4).
Una integrasa ayuda al ADN viral.
(I) Inhibidores de la integrasa
Multiplicación.
El VIH, ya integrado en el ADN de la célula, aprovecha el mecanismo de esta para crear cadenas largas de proteínas del VIH. Con ellas se formarán más copias del VIH.
Cadenas proteínas VIH
Ensamblaje.
El ARN viral y las proteínas producidas por la CD4 salen a la superficie de la célula y se unen a un VIH inmaduro (no infeccioso).
VIH inmaduro
Célula CD4 (huesped)
Gemación.
El nuevo VIH libera proteasa, una enzima del VIH, que se descompone en cadenas de proteínas que hacen maligno el virus.
(I) Inhibidores de la proteasa
VIH maduro e infeccioso
(virus de la inmunodeficiencia humana)
ARN del virus
Enzimas necesarias para replicarse
– Transcriptasa inversa
– Integrasa
– Proteasa
INFECTA….
Células CD4
Tipo de linfocitos que activan el sistema inmunitario en caso necesario ante la presencia de infecciones u otras enfermedades.
INACTIVADORES (I)
Hay varias clases de medicamentos que inactivan el virus en diferente etapas de su ciclo de vida
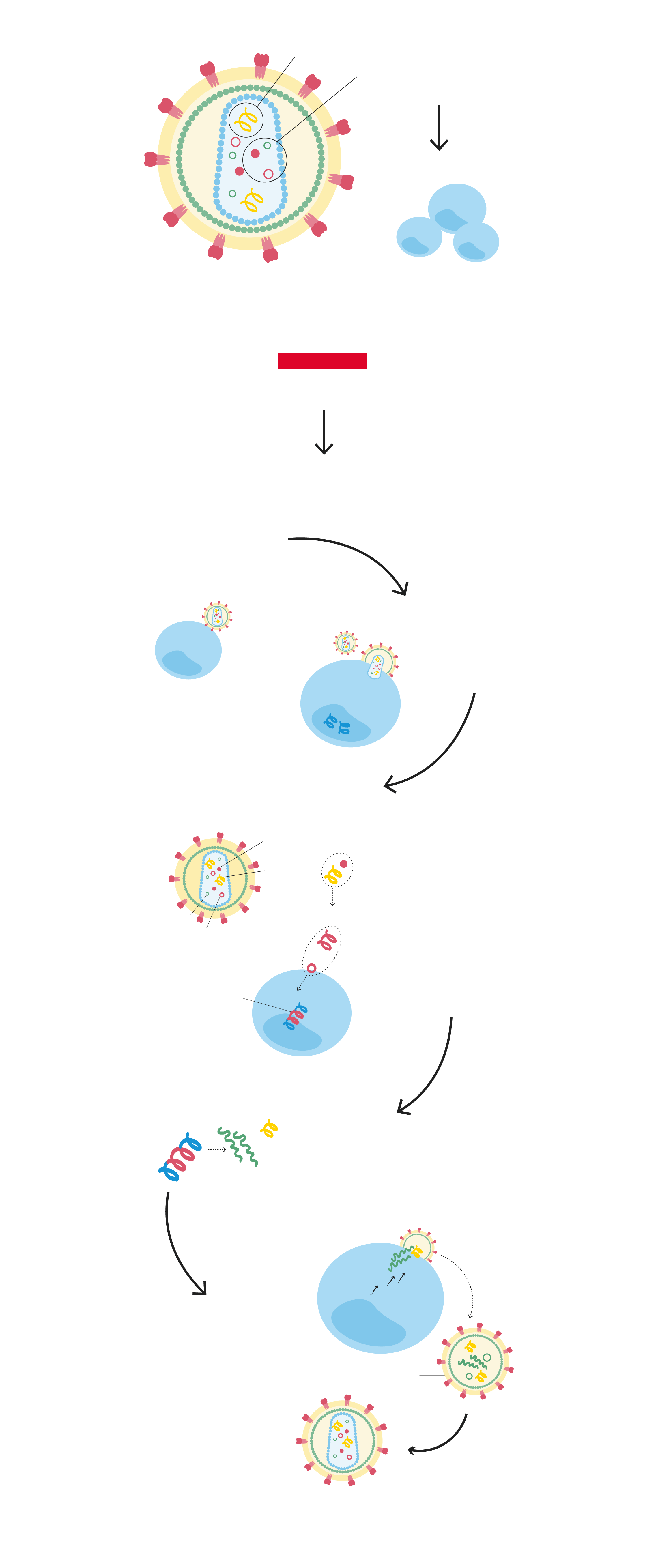
Enlace.
El VIH se fija a los receptores en la superficie del CD4.
(I) Antagonistas de CCR5 (bloquean para que no entre el VIH)
(I) Inhibidores posfijación
Célula CD4
Fusión.
Permitiendo que el VIH entre en la célula.
(I) Inhibidores de la fusión
Transcripción inversa.
Esta enzima convierte el ARN del VIH en ADN, para así poder entrar en el núcleo del linfocito CD4.
(I) Inhibidores de la transcriptasa
Transcriptasa inversa
ARN del virus
ADN del VIH
ADN del VIH
Integración en el genoma del huésped (CD4).
Una integrasa ayuda al ADN viral.
ADN de la CD4
(I) Inhibidores de la integrasa
Multiplicación.
El VIH, ya integrado en el ADN de la célula, aprovecha el mecanismo de esta para crear cadenas largas de proteínas del VIH. Con ellas se formarán más copias del VIH.
Cadenas proteínas VIH
Ensamblaje.
El ARN viral y las proteínas producidas por la CD4 salen a la superficie de la célula y se unen a un VIH inmaduro (no infeccioso).
VIH inmaduro
Célula CD4 (huesped)
Gemación.
El nuevo VIH libera proteasa, una enzima del VIH, que se descompone en cadenas de proteínas que hacen maligno el virus.
(I) Inhibidores de la proteasa
VIH maduro e infeccioso
(virus de la inmunodeficiencia humana)
ARN del virus
Enzimas necesarias para replicarse
– Transcriptasa inversa
– Integrasa
– Proteasa
INFECTA….
Células CD4
Tipo de linfocitos que activan el sistema inmunitario en caso necesario ante la presencia de infecciones u otras enfermedades.
INACTIVADORES (I)
Hay varias clases de medicamentos que inactivan el virus en diferente etapas de su ciclo de vida
Enlace.
El VIH se fija a los receptores
en la superficie del CD4.
(I) Antagonistas de CCR5 (bloquean para que no entre el VIH)
(I) Inhibidores posfijación
Fusión.
Permitiendo que el VIH entre en la célula.
Célula CD4
(I) Inhibidores de la fusión
Transcripción inversa.
Esta enzima convierte el ARN del VIH en ADN, para así poder entrar en el núcleo del linfocito CD4.
(I) Inhibidores de la transcriptasa
Transcriptasa inversa
ARN del virus
ADN del VIH
Integración en el genoma del huésped (CD4).
Una integrasa ayuda al ADN viral.
(I) Inhibidores de la integrasa
ADN del VIH
ADN de la CD4
Multiplicación.
El VIH, ya integrado en el ADN de la célula, aprovecha el mecanismo de esta para crear cadenas largas de proteínas del VIH. Con ellas se formarán más copias del VIH.
Cadenas proteínas VIH
VIH inmaduro
Ensamblaje.
El ARN viral y las proteínas producidas por la CD4 salen a la superficie de la célula y se unen a un VIH inmaduro (no infeccioso).
Célula CD4 (huesped)
Gemación.
El nuevo VIH libera proteasa, una enzima del VIH, que se descompone en cadenas de proteínas que hacen maligno el virus.
VIH maduro e infeccioso
(I) Inhibidores de la proteasa
(virus de la inmunodeficiencia humana)
ARN del virus
Enzimas necesarias para replicarse
– Transcriptasa inversa
– Integrasa
– Proteasa
Células CD4
INFECTA….
Tipo de linfocitos que activan el sistema inmunitario en caso necesario ante la presencia de infecciones u otras enfermedades.
INACTIVADORES (I)
Hay varias clases de medicamentos que inactivan el virus en diferente etapas de su ciclo de vida
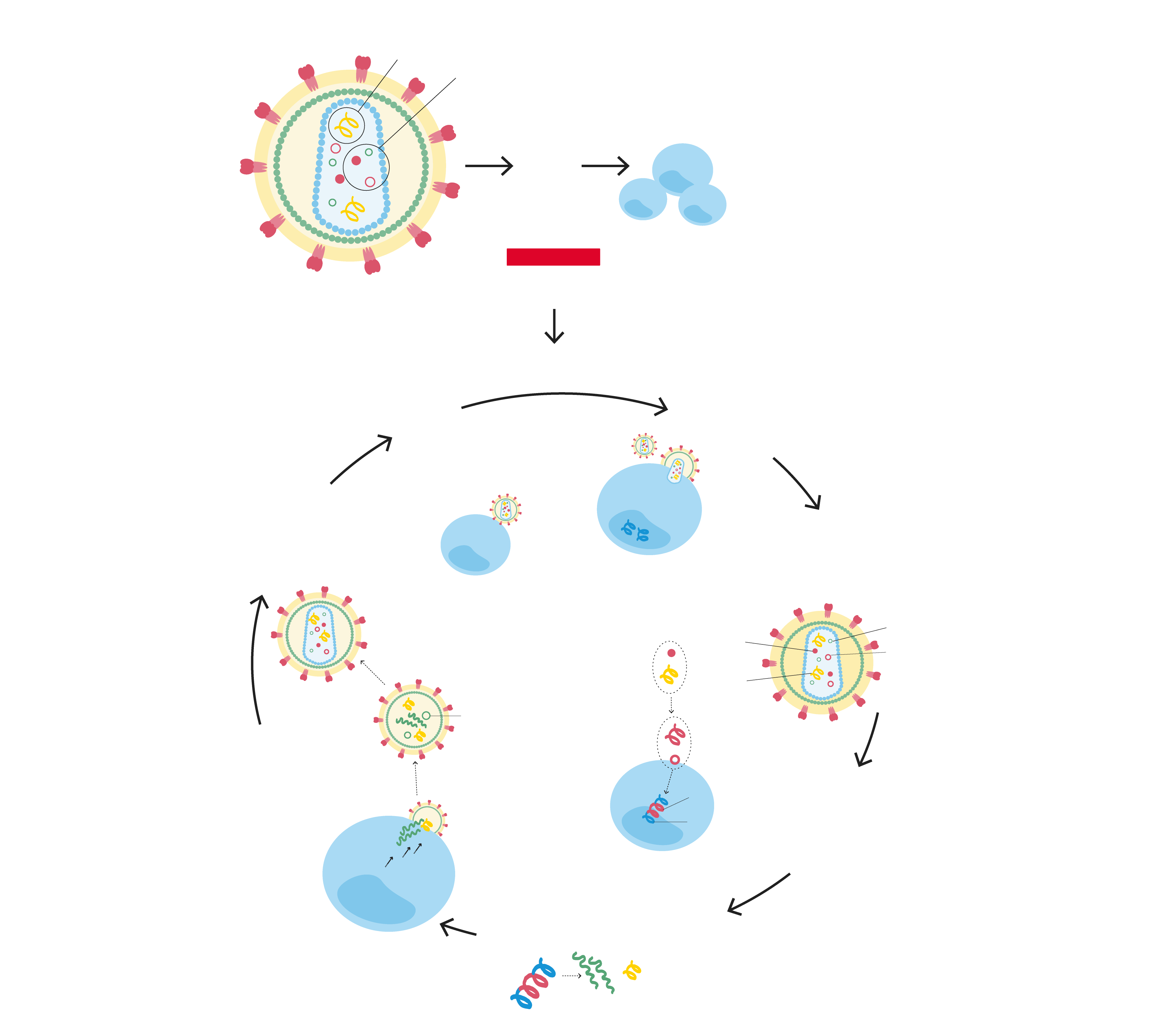
Enlace.
El VIH se fija a los receptores
en la superficie del CD4.
Fusión.
Permitiendo que el VIH entre en la célula.
(I) Antagonistas de CCR5 (bloquean para que no entre el VIH)
(I) Inhibidores de la fusión
(I) Inhibidores posfijación
Gemación.
El nuevo VIH libera proteasa, una enzima del VIH, que se descompone en cadenas de proteínas que hacen maligno el virus.
Transcripción inversa.
Esta enzima convierte el ARN del VIH en ADN, para así poder entrar en el núcleo del linfocito CD4.
Célula CD4
(I) Inhibidores de la proteasa
(I) Inhibidores de la transcriptasa
VIH maduro e infeccioso
Transcriptasa inversa
ARN del virus
ADN del VIH
Ensamblaje.
El ARN viral y las proteínas producidas por la CD4 salen a la superficie de la célula y se unen a un VIH inmaduro (no infeccioso).
Integración en el genoma del huésped (CD4).
Una integrasa ayuda al ADN viral.
ADN del VIH
VIH inmaduro
ADN de la CD4
(I) Inhibidores de la integrasa
Multiplicación.
El VIH, ya integrado en el ADN de la célula, aprovecha el mecanismo de esta para crear cadenas largas de proteínas del VIH. Con ellas se formarán más copias del VIH.
Célula CD4 (huesped)
Cadenas proteínas VIH
Un ataque al ‘corazón’ del virus
El lenacapavir es uno de los aproximadamente 30 antirretrovirales existentes para combatir el virus que provoca el sida. Aprobado por la Administración Estadounidense de Medicamentos (FDA) el 22 de diciembre de 2022 y disponible desde julio en España, lo que le hace diferente es tanto la diana a la que se dirige como la forma de ataque. Sunlenca -su nombre comercial- actúa sobre el ‘corazón’ del VIH, una estructura en forma de cono llamada cápside. En su interior se encuentra la información genética del virus y las enzimas -un tipo de proteínas- que necesita para replicarse. Son la transcriptasa inversa, la integrasa y la proteasa. La primera es la que permite al virus convertir su ARN en ADN cuando infecta a las células del sistema inmunitario, «lo que hace que permanezca en el organismo de por vida. Si se deja el tratamiento, se reactiva». La integrasa es la herramienta que utiliza para insertar su información genética en el genoma de la célula. Y la proteasa es la sustancia que permite su multiplicación. La cápside protege tanto el ARN como las enzimas y además es clave en el transporte del contenido viral hasta la célula.
Doble frente
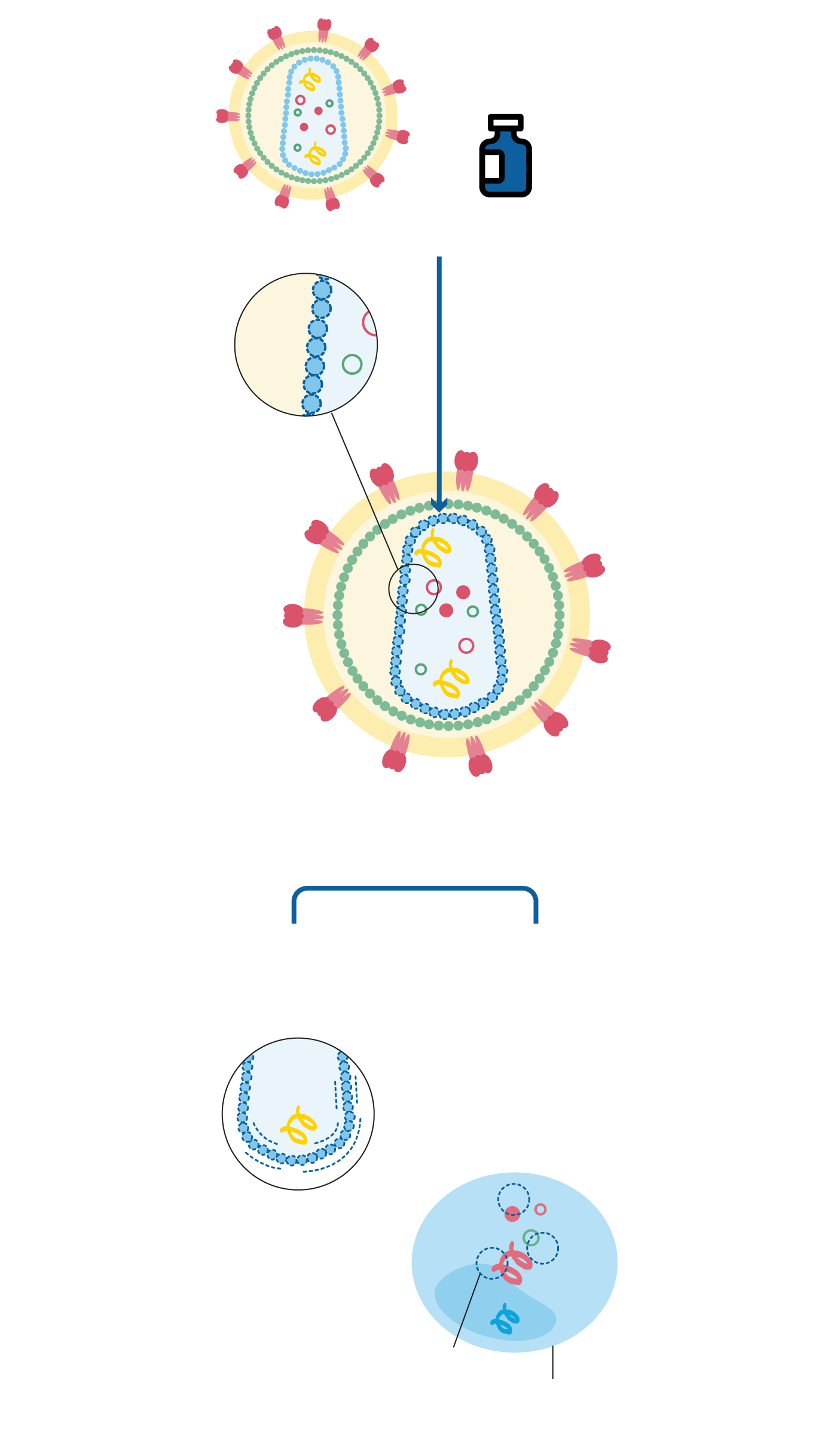
Lo que hace el lenacapavir es unirse a la cápside. «Interacciona con la proteína que forma esta envoltura», explica Menéndez. Con ello consigue dos cosas. La primera, impedir el transporte del ARN viral; la segunda, impedir la maduración de nuevos virus en el interior de la célula infectada si el patógeno ha logrado esquivar el primer ataque. Esta doble acción explica su efectividad incluso frente a cepas resistentes a otros fármacos antirretrovirales. El objetivo de todos ellos es reducir la carga viral -la cantidad de virus en sangre- hasta niveles indetectables. Cuando se consigue esto, el virus no puede ni transmitirse ni dañar al sistema inmunitario.
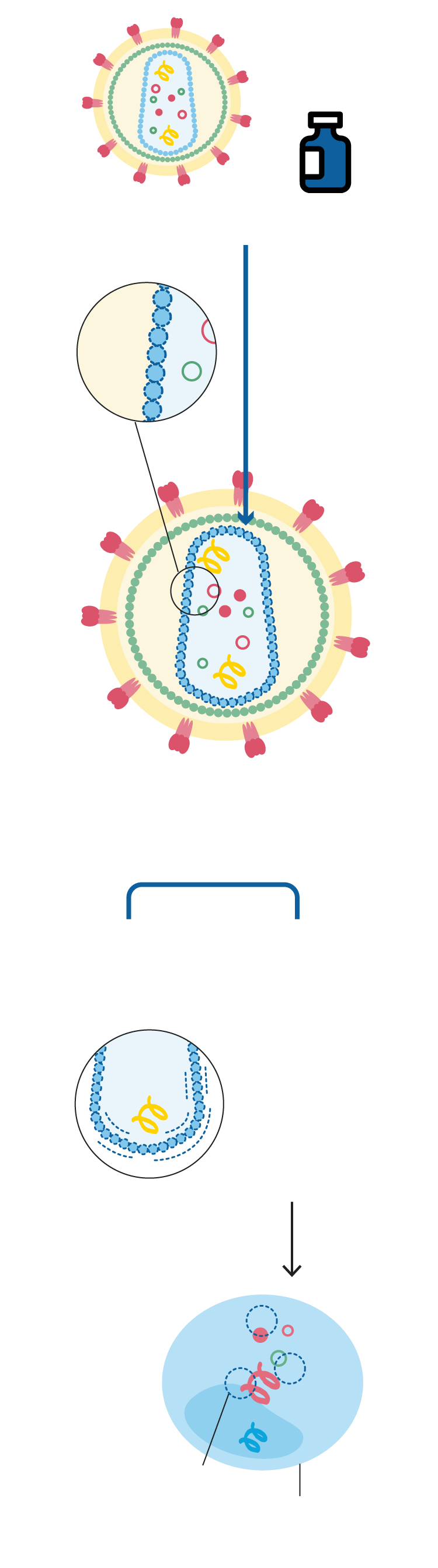
LENACAPAVIR
Se une a la cápside
¿Qué impide?
La maduración de nuevos virus en el interior de la célula infectada si el patógeno ha logrado esquivar el primer ataque.
El transporte del ARN viral
Interacciona con la proteína que forma la envoltura de la cápside.
Lenacapavir impide la maduración
Célula CD4
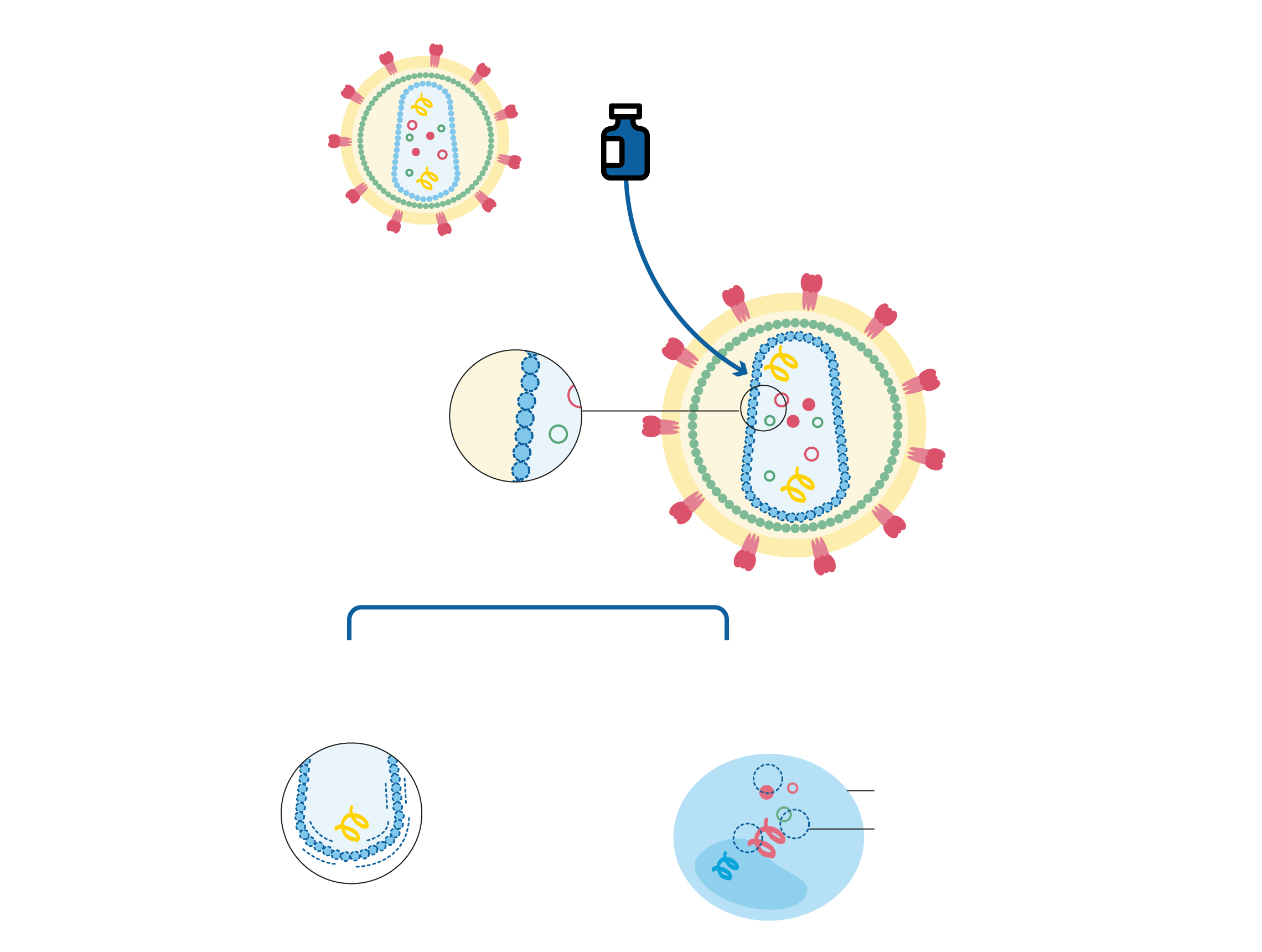
LENACAPAVIR
Se une a la cápside
¿Qué impide?
La maduración de nuevos virus en el interior de la célula infectada si el patógeno ha logrado esquivar el primer ataque.
El transporte del ARN viral
Interacciona con la proteína que forma la envoltura de la cápside.
Lenacapavir impide la maduración
Célula CD4
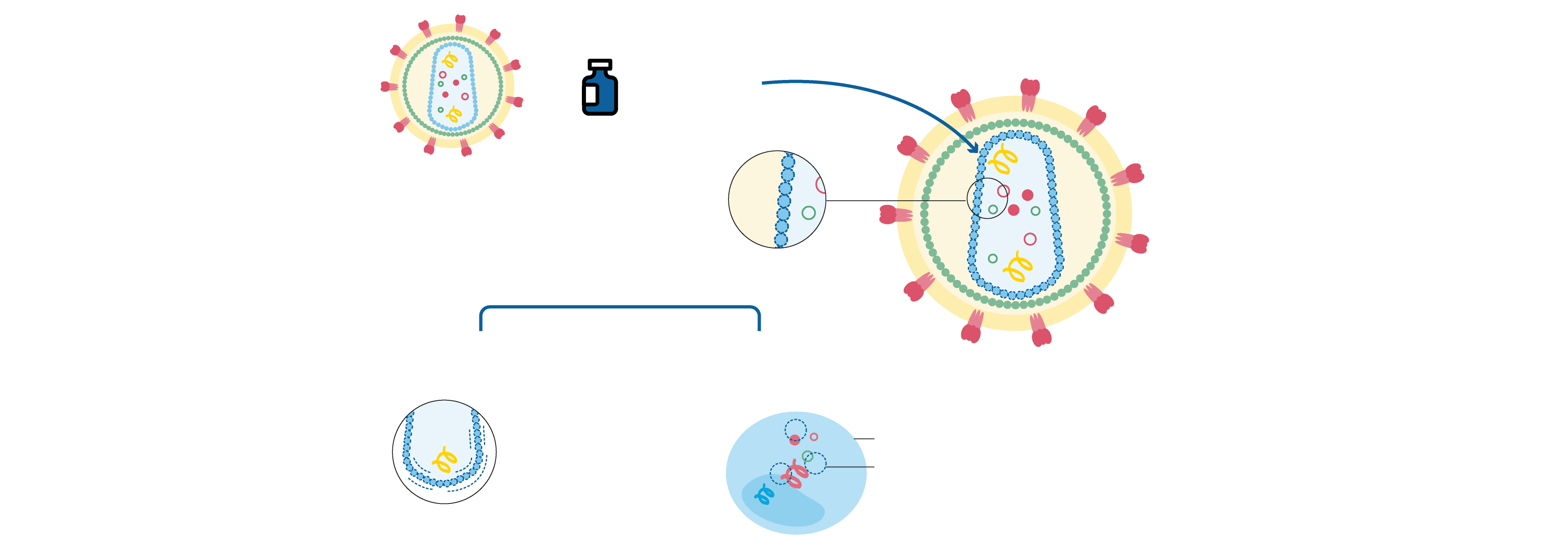
LENACAPAVIR
Se une a la cápside
¿Qué impide?
El transporte del ARN viral
La maduración de nuevos virus en el interior de la célula infectada si el patógeno ha logrado esquivar el primer ataque.
Célula CD4
Lenacapavir impide la maduración
Interacciona con la proteína que forma la envoltura de la cápside.
LENACAPAVIR
Se une a la cápside
¿Qué impide?
La maduración de nuevos virus en el interior de la célula
infectada si el patógeno ha logrado esquivar el primer ataque.
El transporte del ARN viral
Interacciona con la proteína que forma la envoltura de la cápside.
Célula CD4
Lenacapavir impide la maduración
Las armas del VIH
El VIH pertenece a una gran familia de virus llamada retrovirus. Su principal característica es la mencionada capacidad para convertir su ARN en ADN e insertar este en el código genético de la célula infectada. Son las CD4, unas células del sistema inmune encargadas de organizar la respuesta defensiva ante las infecciones. De esta forma acaba debilitando el organismo hasta hacerlo vulnerable a cualquier patógeno.
Otra razón que explica su resistencia a las vacunas es que a diferencia de otros microbios como el coronavirus, «esconde la ‘llave’ sobre la que actúan los anticuerpos. Y cuando la enseña para entrar en las células, el espacio es demasiado pequeño para los anticuerpos», asegura el virólogo José Alcamí.
Efectividad

Su capacidad para combatir la infección ronda el 83%, similar a la de otros antirretrovirales. Lo que le hace extraordinario es su poder profiláctico. En junio de este año, un gran ensayo clínico descubrió que el lenacapavir previno completamente la infección en niñas adolescentes y mujeres jóvenes africanas. En noviembre, las pruebas se hicieron en personas de género diverso que mantienen relaciones con otros hombres.
La efectividad fue del 99,9%: solo dos de los 2.180 voluntarios se contagiaron. Su efecto protector se prolonga durante seis meses, más que cualquier otro antirretroviral. «Es su gran logro y algo totalmente inesperado. Tiene el efecto de una vacuna a corto plazo», destaca el profesor del Severo Ochoa.
Administración
La administración es otra de sus grandes ventajas. A diferencia de la mayor parte de tratamientos, que han de tomarse todos los días por vía oral, el lenacapavir se inyecta cada medio año, lo que limita lo que los especialistas llaman adherencia, es decir, cumplir a rajatabla el tratamiento. «El objetivo es evitar que se replique para que no genere resistencias con las mutaciones».
Como el resto de fármacos de este tipo, se toma en forma de cóctel, mezclado con al menos otros dos antirretrovirales, para impedir que las mutaciones del virus esquiven los efectos del tratamiento. «Si solo incidieran en una diana, con una o dos mutaciones el virus podría generar resistencia. Con cada nueva diana se multiplican las opciones de que no lo logre», incide Menéndez.
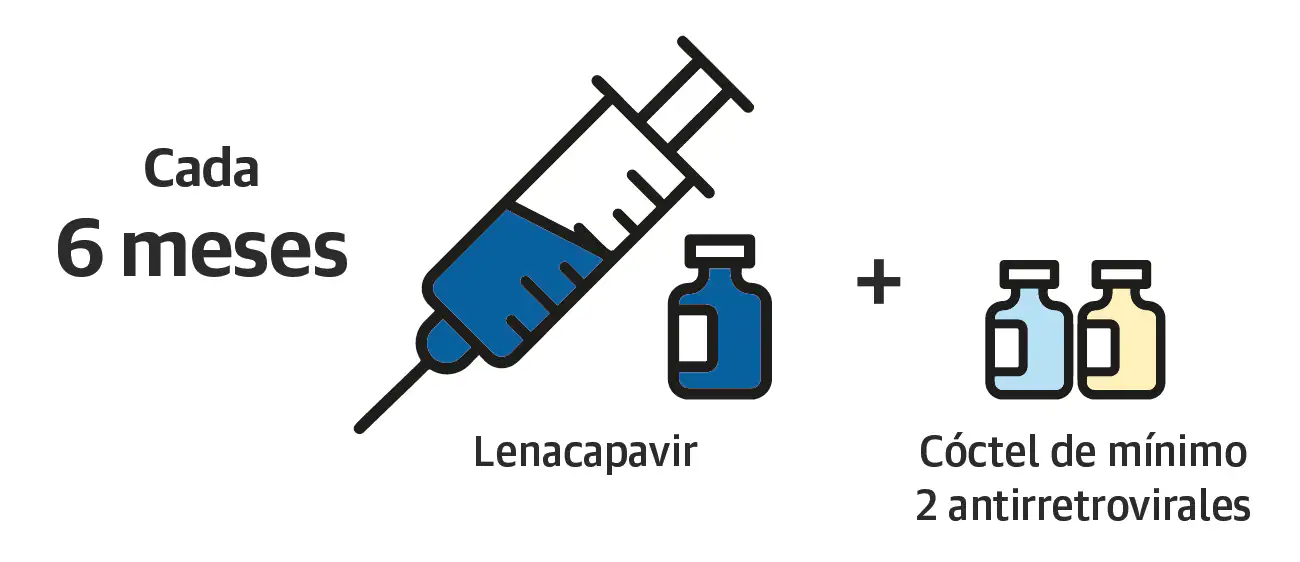
Por el momento está pautado para los casos de pacientes en los que no son efectivos otros fármacos. Su uso preventivo todavía no está aprobado aunque se espera que lo sea a finales de 2025. Su mayor ‘pero’ es su precio: la farmacéutica norteamericana Gilead cobra 40.000 dólares -38.400 euros- al año por paciente, aproximadamente cuatro veces más que el tratamiento antirretroviral más costoso en la actualidad.

Soy William Abrego, me uní como ejecutivo de SEO y me abrí camino hasta el puesto de Gerente Asociado de Marketing Digital en 5 años en Prudour Pvt. Ltd. Tengo un conocimiento profundo de SEO en la página y fuera de la página, así como herramientas de marketing de contenido y diferentes estrategias de SEO para promover informes de investigación de mercado y monitorear el tráfico del sitio web, los resultados de búsqueda y el desarrollo de estrategias. Creo que soy el candidato adecuado para este perfil ya que tengo las habilidades y experiencia requeridas.
Enlace de origen : Así actúa el medicamento elegido como avance científico del año



